
노바백스사의 코로나19 백신(뉴백소비드프리필드시린지, 이하 노바 백신)이 오늘 1월 12일 국내 사용승인을 받았습니다. 노바 백신은 화이자나 모더나 백신에 비해 안전성이 뛰어나 많은 관심을 받고 있는데 한 번 살펴보도록 하겠습니다.
먼저 알아둬야 할 사실은 노바백신이 기본접종으로 승인이 났다는 점이다. 이는 미접종자의 1, 2차 기본접종에 쓰이며 이미 다른 백신을 맞은 접종자의 추가접종 승인은 나지 않았다. 차후 임상전문가들과의 논의를 통해서 추가접종 여부를 결정한다고 합니다. 다만, 추가접종 승인이 받지 못했더라도 허가범위 외로 사용되는 의약품을 적용해서 추가접종으로 사용될 수 있다는 입장을 밝혔다.
국내에서 사용하게 될 노바 백신은 sk바이오사이언스에서 제조되는 백신이며, 21일 간격으로 2회 접종하게 됩니다. 그리고 화이자나 모더나처럼 1개의 백신병에 희석제를 섞어서 나눠 주사하는 게 아니라 한 개의 병에 1회 용량이 들어있어 희석 소분 없이 바로 주사하게 됩니다. 보관조건도 냉장(2~8℃)에서 5개월이라 모더나 화이자보다 훨씬 용이하네요. 아래는 정부 보도자료입니다.
□ 식품의약품안전처(처장 김강립)는 SK바이오사이언스(주)가 제조판매품목 허가를 신청한 코로나19 백신 ‘뉴 백소 비드 프리필드 시린지’에 대해 1월 12일 임상시험 최종결과보고서 등을 제출하는 조건으로 품목허가를 결정했습니다.
제품 개요 및 허가 의의
□ ‘뉴백소비드프리필드시린지’는 미국 노바백스사(社)가 개발하고, 국내 SK바이오사이언스(주)에서 원액부터 완제까지 제조하는 유전자 재조합 코로나19 백신입니다.
○ 유전자재조합 백신은 재조합 기술을 이용해 만든 항원 단백질을 직접 주입하여 체내에서 바이러스에 대항할 수 있는 항체 생성을 유도하는 방식으로, 이미 B형 간염, 자궁경부암 백신 등의 제조에 사용되고 있습니다.
□ 효능‧효과는 18세 이상에서 코로나19의 예방이고, 용법‧용량은 0.5mL을 21일 간격으로 2회 접종하며, 주성분이 유럽 등 30개국과 WHO에서 조건부 허가 또는 긴급사용승인받은 백신(10회 용량이 포장된 바이알)과 동일합니다.
※ (조건부허가) 유럽(EMA) 27개국
(긴급사용승인) 세계보건기구(WHO), 인도, 인도네시아, 필리핀
○ 이 백신은 백신 1개당 1회 용량이 포함된 프리필드시린지 형태의 1인용 주사제로 희석 또는 소분 없이 바로 접종할 수 있으며, 보관조건은 냉장(2~8℃)에서 5개월입니다.
□ 식약처는 ‘뉴백소비드프리필드시린지’가 ▲국민들께서 접종 경험이 있는 유전자재조합 방식으로 제조되었다는 점 ▲보관, 수송, 사용이 편리한 점 ▲의료현장에서 선택할 수 있는 백신 종류가 확대되었다는 점에서 의미가 있다고 평가하였습니다.
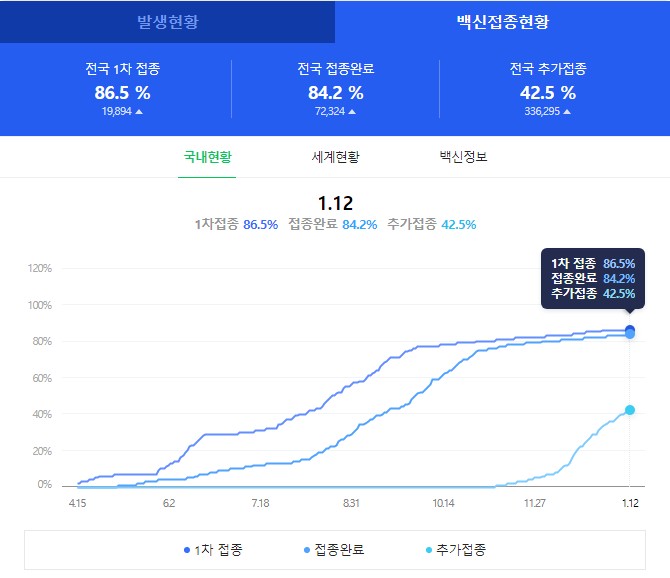
오늘 갑자기 확진자 확 늘었다. 많이 힘들고 지친다. 이제 치료제도 들어오고 새로운 백신도 곧 접종을 시작하게 된다. 하루 빨리 조용하게 평화롭게 살 수 있는 날이 왔으면 좋겠다.
'일상리뷰' 카테고리의 다른 글
| 스톤힐 노트북 받침대 리뷰! 거북목 척추건강이 걱정된다면 (0) | 2022.02.05 |
|---|---|
| 빅데이터 통계에 관심있다면 무료로 교육받으세요~ 통계무료교육! 통계교육원! (0) | 2022.01.30 |
| 노바백스 백신 승인! 우리 아이들 접종 가능할까? (0) | 2022.01.08 |
| M1 맥북 에어 13 -최고의 가성비 노트북! 둘러보기! (0) | 2022.01.08 |
| 너프건 고장! 너프건 수리(self) 후기 (feat. RUKKUS ICS-9) (0) | 2022.01.07 |



